原發性中樞神經系統血管炎(PACNS)是中樞神經系統(腦、脊髓和腦膜)特有的炎症性血管病,由於缺乏特異性生物標誌物,臨床診斷比較困難,影像上很難與其他疾病鑒別,主要是通過排除其他疾病而進行診斷。本文將重點談談PACNS和他的mimickers。
01
PACNS
PACNS是一種罕見的自身免疫性疾病,病因不明,多發於中樞神經系統的中小血管。血管局部變窄或閉塞,導致組織缺血和甚至壞死。PACNS主要有三種病理類型:肉芽腫性血管炎(最常見)、淋巴細胞性血管炎、壞死性血管炎。
PACNS的年發病率為2.4/100萬,男性比例稍高,多見於60歲人群。PACNS的急性表現通常包括缺血性或出血性卒中,導致新的局灶性神經功能缺損,如共濟失調、失語、感覺改變、輕癱或麻痹。最常見的症狀是隱匿性頭痛和精神錯亂,其他非特異性表現還有發熱、噁心、帕金森病或脊髓病。
PACNS的檢查包括血液檢查、頭顱MRI、腰椎穿刺(LP)、數位減影血管造影(DSA)和活檢。雖然目前還沒有針對PACNS的特異性血液檢測,但所選檢查主要用於排除PACNS的mimickers。在PACNS中,由於炎症反應局限於中樞神經系統,血沉(ESR)和C反應蛋白(CRP)通常在正常范圍。
頭顱MRI是PACNS最敏感的檢測方法,但仍無特異性。但國內學者納入18例PACNS的研究[1]顯示雙側病灶較單側病灶多見;最常受累部位為額葉,其次為頂葉和枕葉;皮質下白質常受累,而基底節、腦膜和脊髓則不常見。由於PACNS通常累及中小血管,DSA通常表現為「串珠」樣改變,偶爾會發現動脈瘤。血管壁磁共振成像(VW-MRI)有助於PACNS的診斷,VW-MRI的特徵為平滑性向心性增強以及受累動脈增厚(圖1)。LP常見腦脊液細胞增多和蛋白質升高。PACNS的金標準診斷是腦活檢。但活檢的敏感性只有50%,受限於疾病的斑塊性質和活檢技術。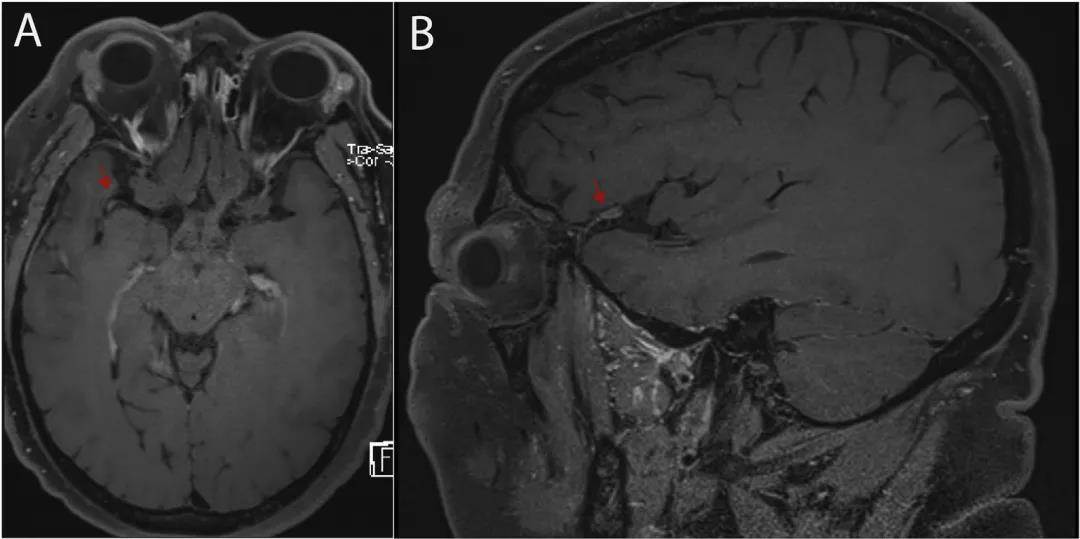
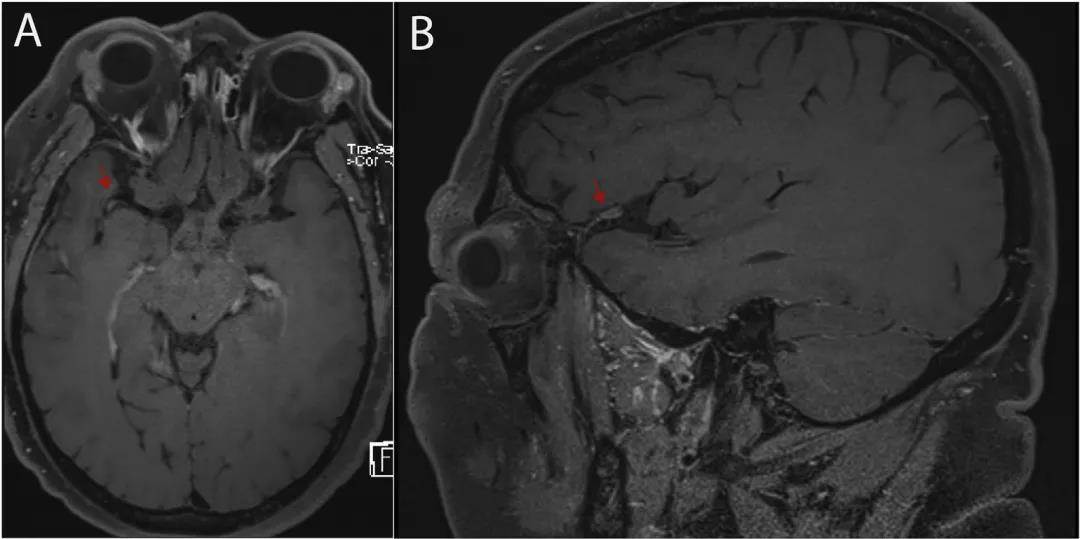
圖1 一例PACNS患者的資料
A和B:T1軸位(A)和矢狀位元(B)顯示外側裂內右側大腦中動脈血管壁增強(箭頭)。
圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569[2]
關於PACNS的診斷,Calbrese和Malle提出了簡單的標準:
➤ 獲得性神經功能缺損的臨床表現,經全面評估仍無法用其他病因解釋;
➤ PACNS的典型血管造影(串珠樣改變)或組織病理學表現;
➤ 無系統性血管炎的證據。儘管這些標準很簡單,但在實踐中,由於DSA和活檢的敏感性差而導致診斷仍然是一個挑戰。
為此,有研究[3]總結了24個病例系列研究得出結論:
➤ 主要臨床特徵(≥42.7%):頭痛、卒中、認知障礙和局灶性神經功能缺損;
➤ 次要臨床特徵(<42.7%):癲癇發作、意識水準改變、精神障礙;
➤ 主要影像學特徵(≥46.6%):多發實質病變、實質或腦膜增強、血管異常(單個或多個狹窄/閉塞)和血管壁增強;
➤ 次要影像學特徵(<46.6%):實質性或蛛網膜下腔出血,單個實質病變。
如果患者有:1個臨床特徵(主要或次要)和一個主要影像學特徵,或兩個臨床特徵(至少一個為主要特徵)和一個次要影像學特徵,並不能用其他病因解釋,則應初步懷疑PACN。
PACNS的治療包括大劑量皮質類固醇(甲基強的松龍1 g靜脈注射5天,然後強的松1 mg/kg/d至少持續4周,然後緩慢減量)和環磷醯胺(15 mg/kg,每2週一次,共3次;接下來每3週一次,共3次)。包括霉酚酸酯、硫唑嘌呤和利妥昔單抗在內的各種免疫抑制劑已被用於維持病情緩解。
02
RCVS
可逆性腦血管收縮綜合征(RCVS)是一種可逆性、非炎症性、自限性CNS動脈病變,導致多灶節段性腦血管收縮,隨後出現正常動脈或舒張血管。
RCVS的發病率目前尚不清楚,但據估計遠高於PACNS,平均發病年齡為40歲,女性比例高於男性。RCVS急性期表現為嚴重的突發性頭痛,稱為雷擊性頭痛,伴或不伴其他神經症狀,包括輕癱、感覺改變、視力改變或失語。缺血性卒中、出血性卒中、蛛網膜下腔出血、癲癇發作甚至死亡較少見。RCVS的病理生理學尚不清楚,可能與動脈血管壁張力改變,引起血管局部性波動性收縮有關。RCVS的組織病理學為非特異性表現,無炎症病變。RCVS常因各種觸發因素而發生,包括藥物、高血壓、[吸·毒]和產後狀態;可能的藥物包括選擇性血清素再攝取抑制劑(如帕羅西汀)、止咳藥或麥角胺、可卡因、大麻、安非他明及其衍生物和搖頭丸等非法藥物;其他不太常見的觸發因素包括情緒壓力、近期手術、[性.交]、洗澡和高海拔地區;一些患者也可以沒有觸發因素。
對於RCVS,首先應進行頭顱CT以排除蛛網膜下腔出血或其他可能導致神經狀態突然改變的病因。DSA可用於尋找RCVS的典型表現:節段性和多灶性血管收縮和腦動脈擴張(圖2A)。CTA和MRA常能在無創性、風險小的情況下,鑒別病變類型並作出診斷。MRI對於RCVS的評估必不可少,但多達1/3的RCVS患者可有正常MRI表現,異常表現包括FLAIR序列上的「點征」
,出現在腦溝間隙,可能是腦血流減慢所致,或RCVS導致的梗死區域(圖2B)。LP對RCVS的診斷必不可少,一是有助於排除頭顱CT陰性的隱匿性蛛網膜下腔出血,二是有助於評估血管病變的其他可能病因,如PACNS。一般來說,RCVS患者的CSF正常或輕度異常(總蛋白輕度升高)。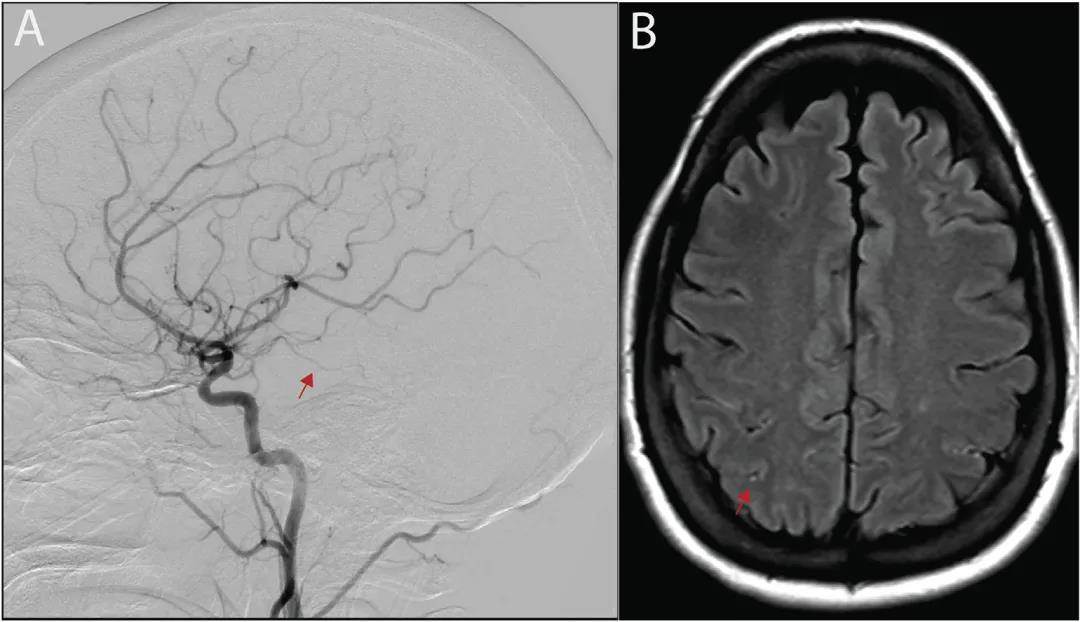
圖2 一例RCVS患者的資料
A:DSA顯示多灶性動脈不規則;B:FLAIR序列顯示 「點」征。
圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569.
有研究[4]對RCVS和PACNS進行了比較:兩者頭痛都很常見,但RCVS的頭痛發病突然,通常為雷擊樣頭痛,而PACNS起病隱匿,頭痛性質為鈍痛,並伴神經功能缺損;局灶性功能缺陷如偏癱和失語在PACNS中更為常見,而Balint綜合征和皮質視覺症狀在RCVS中很常見;RCVS患者可有正常的神經影像學表現,而PACNS患者入院時腦部掃描基本有異常;RCVS中的梗死位於淺表交界區或分水嶺區,通常不累及皮質,很少累及深部結構,而PACNS患者有播散性小梗死和微血管病性白質改變,與遠端動脈的彌漫性受累相一致。
近期有研究[5]提出了RCVS2評分系統(表1)用於RCVS的診斷,評分≥5 診斷RCVS的特異性為99%,敏感性為90%;評分≤2排除RCVS的特異性為100%,敏感性為85%;評分3–4 診斷RCVS的特異性為86%,敏感性為10%。
表1 RCVS2 評分系統

注:血管收縮誘發因素:藥物、產後、[性.高.潮]
關於RCV的治療,目前尚缺乏隨機對照試驗的證據,主要基於專家意見。一些專家建議支持性治療和寬鬆的血壓管理,因為大多數患者會自行恢復,血壓下降或升高可能會帶來缺血或再灌注損傷的風險。其他專家建議口服鈣通道阻滯劑,如尼莫地平和維拉帕米作為一線藥物。糖皮質激素,通常在懷疑PACNS時經驗性使用,但可能會加重RCVS,通常需避免。
03
Sneddon綜合征
Sneddon綜合征包括網狀青斑和缺血性卒中或短暫性腦缺血發作,該病是一種罕見的血管病,年發病率為4/100萬人,最常見於20-42歲年輕女性,男女比例為1:5。
Sneddon綜合征的潛在病因尚不清楚,自身免疫可能是機制之一,自身免疫引起內皮功能障礙,最終導致中小血管充血和血栓形成。該病與抗磷脂抗體綜合征、系統性紅斑狼瘡、瓣膜病和遺傳易感性有關,約50%-80%的患者抗磷脂抗體也呈陽性。
Sneddon綜合征的診斷主要是基於皮膚病和卒中病史的同時發生(圖3)。實驗室檢查應包括抗磷脂抗體、系統性紅斑狼瘡和其他高凝狀態原因的篩查。MRI在急性期可見梗死灶,慢性期在T2/FLAIR上有異常信號改變,通常位於腦室周圍深部白質和橋腦。DSA在75%的Sneddon綜合征病例中發現典型的血管病變,最常見的是閉塞性非炎性動脈病變,伴有顱內血管狹窄和/或閉塞。皮膚病理學可見內膜內皮細胞增生和中層平滑肌細胞增生導致皮下小動脈血栓形成,毛細血管代償性擴張導致血流受損,導致網狀青斑。Sneddon綜合征患者通常不需要進行腦活檢,但當進行腦活檢時,最突出的發現包括非特異性血管病,中小血管內膜增厚,動脈血栓形成,而沒有炎症病變。
Sneddon綜合征的治療方案包括抗血小板治療或抗凝治療。也有研究使用免疫抑制劑進行治療,但療效不一;而高血壓和激素暴露與疾病進展有關。

圖3 一例Sneddon綜合征患者的資料
A:皮膚網狀青斑(星號);B:皮膚活檢顯示毛細血管內廣泛血栓形成;比例尺100μm;C:FLAIR/T2 MRI顯示多發性缺血性病變(白色箭頭)和皮質萎縮(紅色箭頭)。
圖片來源於Orphanet J Rare Dis . 2014 Dec 31;9:215.
04
ABRA
腦澱粉樣血管病(CAA)是一種非炎症性疾病,由β澱粉樣蛋白沉積於大腦中、小動脈和軟腦膜血管的肌外膜和中膜所致。β澱粉樣蛋白的沉積導致血管變得脆弱,容易出血。幾乎所有的CAA患者都有亞臨床實質和蛛網膜下腔微出血。對澱粉樣沉積的免疫反應導致血管內或血管周圍的炎症反應,分別稱為β澱粉樣蛋白相關血管炎(ABRA)和CAA相關炎症。
ABRA是一種血管破壞性病變,伴跨壁炎症,病理檢查常可見肉芽腫。ABRA的發病率尚不清楚,男女比例相等,大多數ABRA患者年齡≥50歲,而PACNS患者中有一半在這個年齡之前出現。。ABRA最常見的表現包括行為改變和亞急性認知能力下降,特別是幻覺,其他常見表現包括局灶性無力、感覺改變、癲癇發作、頭痛、共濟失調或失語。由於脊髓血管免於β澱粉樣蛋白沉積,ABRA一般無脊髓病症狀,如果出現,更應考慮PACNS。
MRI對於ABRA尤為重要,常見的MRI表現包括不對稱T2高信號延伸至皮質旁區域,有研究提示後迴圈更容易受累,但也有研究顯示額葉更常見;增強序列可見特徵性的軟腦膜強化,反映軟腦膜小血管受累;磁敏感加權成像顯示微出血(圖4)和甚至腦葉出血。其他檢查包括血清炎症標誌物,如血沉和CRP,偶爾升高。腦脊液有蛋白升高,輕度細胞增多。寡克隆帶與ABRA無關。重要的是DSA通常正常。ABRA的診斷通常是在組織病理學檢查證實跨壁炎症和血管壁中持續存在β澱粉樣蛋白後確診(圖5)。
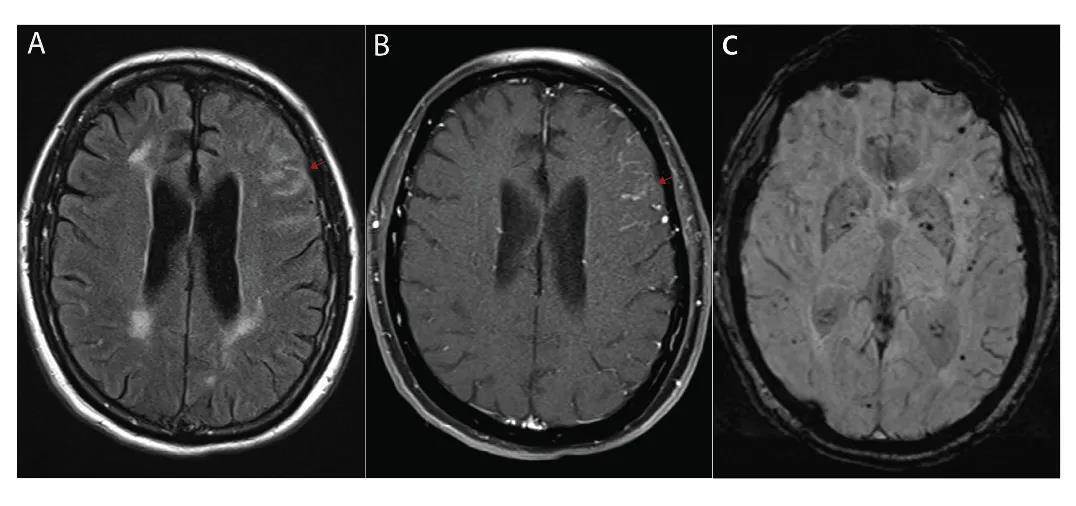
圖4 一例ABRA患者的資料
A:FLAIR顯示左側額葉溝T2無抑制;B:T1增強顯示同一區域相應的局灶性軟腦膜增強。C:SWI顯示多灶性磁敏感偽影(blooming artifact)。
圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569.
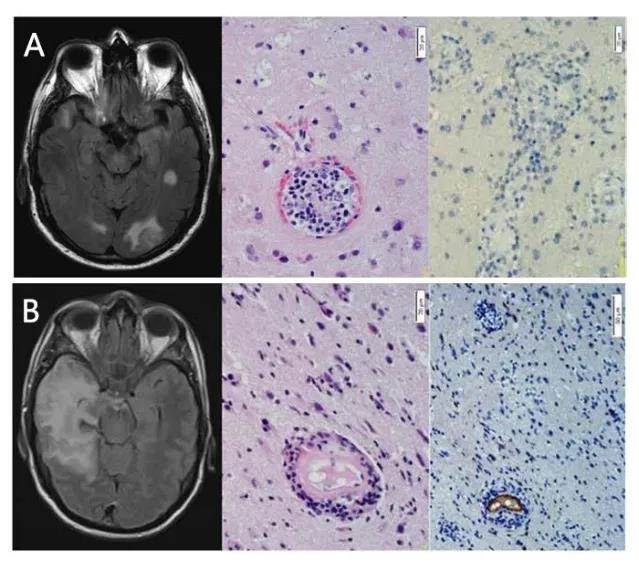
圖5 一例PACNS和一例ABRA患者的資料
A:PACNS患者頭顱MRI顯示T2高信號病灶,病理檢查可見淋巴細胞浸潤血管、細胞壁壞死和紅細胞外滲,但無β澱粉樣蛋白沉積;B:ABRA患者頭顱MRI顯示T2高信號病灶,病理檢查可見淋巴細胞和肉芽腫浸潤血管,纖維蛋白樣壞死,有β澱粉樣蛋白沉積。圖片來源Stroke, 2015 Sep;46(9):e210-3.
ABRA的治療是基於專家的意見,通常參照PACNS的治療方案。大多數患者接受大劑量皮質類固醇治療(甲基強的松龍1 g靜脈注射5天,然後1mg/kg/d的強的松,並在4-8周內逐漸減量)。對於嚴重的病例,有時會使用環磷醯胺。與PACNS相比,一些ABRA患者的病程呈單相,僅需短期服用大劑量皮質類固醇。
05
Susac綜合征
Susac綜合征是一種罕見的血管病,影響大腦、內耳和視網膜的小動脈,導致缺血性卒中、聽力喪失和視力喪失。該病女性多見(3.5:1),年齡在30-40歲之間。Susac綜合征的臨床表現是病變組織小血管閉塞的結果,但血管閉塞機制尚不清楚,很可能是一種自身免疫過程。
Susac綜合征常見的神經症狀包括認知障礙、頭痛、困惑、情緒障礙、行為改變和冷漠。
發病初期,患者通常沒有完整的三聯症狀,一般在病程21周時出現三聯症。Susac綜合征急性期的典型MRI表現是胼胝體「雪球病變」(圖6),其他MRI表現包括缺血性卒中,表現為小面積的彌散受限和軟腦膜增強;慢性期MRI表現包括小的T1低信號病變、萎縮和胼胝體變薄。視網膜螢光素血管造影進行眼科檢查通常顯示視網膜分支動脈閉塞(BRAO)和血管壁高螢光。聽力檢查顯示感音神經性聽力損失。腰椎穿刺非必需,但通常用於排除其他原因;Susac綜合征的CSF通常是非特異性的,通常表現為蛋白升高,有時細胞輕度升高(平均約12個白細胞),很少有寡克隆帶。
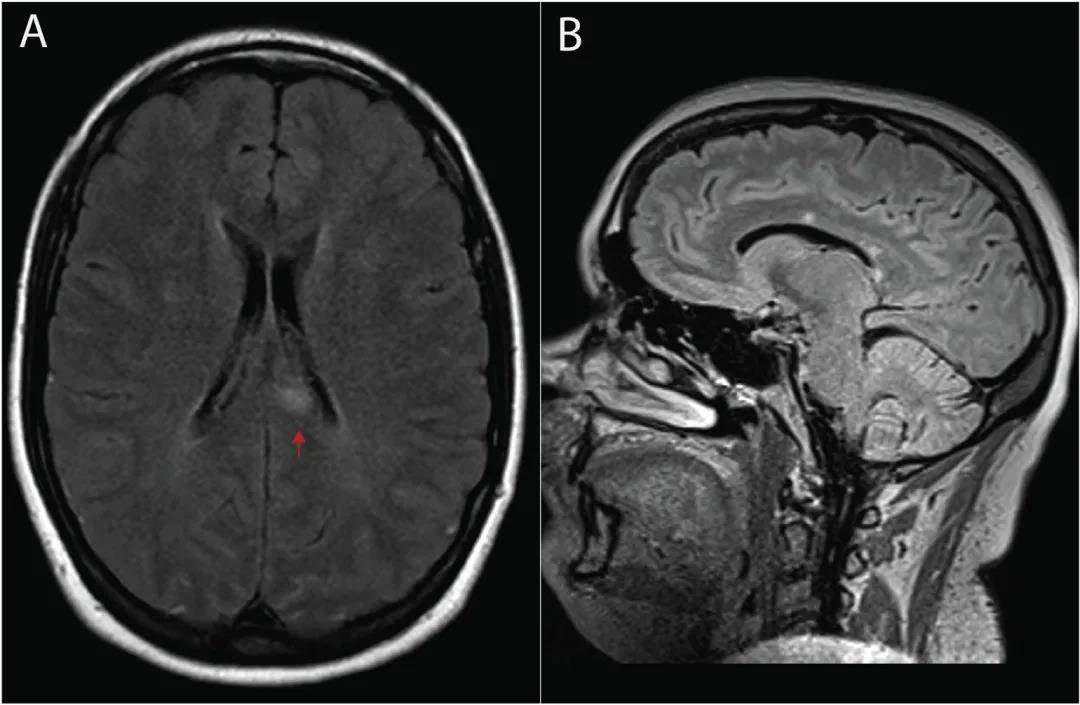
圖6 一例Susac綜合征患者的資料
A和B:MRI FLAIR序列軸位(A)和矢狀位元(B)影像顯示胼胝體高信號「雪球」樣病灶。圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569.
有研究[6]對13例Susac綜合征和15例PACNS進行比較認為:Susac綜合征患者認知障礙、共濟失調和聽覺障礙相對於PACNS更為常見;而在PACNS患者中,癲癇發作更為常見。
胼胝體(CC)受累多見於Susac綜合征,13例Susac綜合征患者中有13例CC膝異常,而15例PACNS患者中只有2例CC膝異常(p<0.001);13例Susac綜合征患者中有13例CC體受累,15例PACNS患者中有1例CC體受累(p<0.001);皮質病變、出血和基底節梗死在PACNS患者中更為常見。但總的來說,Susac綜合征的診斷還沒有正式的標準,主要是基於三聯症並排除其他原因。Susac綜合征的治療是基於專家意見,類似於PACNS,用大劑量皮質類固醇加或不加環磷醯胺(或利妥昔單抗)。
06
CADASIL
伴有皮質下梗死和白質腦病的常染色體顯性遺傳性腦動脈病(CADASIL)是常染色體顯性遺傳模式導致非炎症性血管病,男女發病率相等,最常見於歐洲高加索家庭。
CADASIL是因染色體19p13基因突變導致NOTCH3蛋白缺陷,引起血管中的跨膜受體功能障礙,導致顆粒和嗜鋨物質與Notch3本身在血管平滑肌壁上積聚。儘管存在於全身的血管中,但主要影響大腦小動脈(動脈病變)。患者通常表現為偏頭痛,最常見於60歲人群,也可出現缺血性卒中;其他表現包括認知改變、癡呆、個性改變和抑鬱。
CADASIL典型的影像學表現為白質T2加權/FLAIR序列高信號改變,彌散加權成像顯示皮質下梗死,磁敏感性加權成像顯示腦微出血。最常受累及的區域有腦室周圍區域、前顳極、外囊以及額葉和頂葉區域(圖7)。MRI改變的嚴重程度與症狀的嚴重程度直接相關,並且MRI改變通常發生在臨床症狀出現前10年15年。
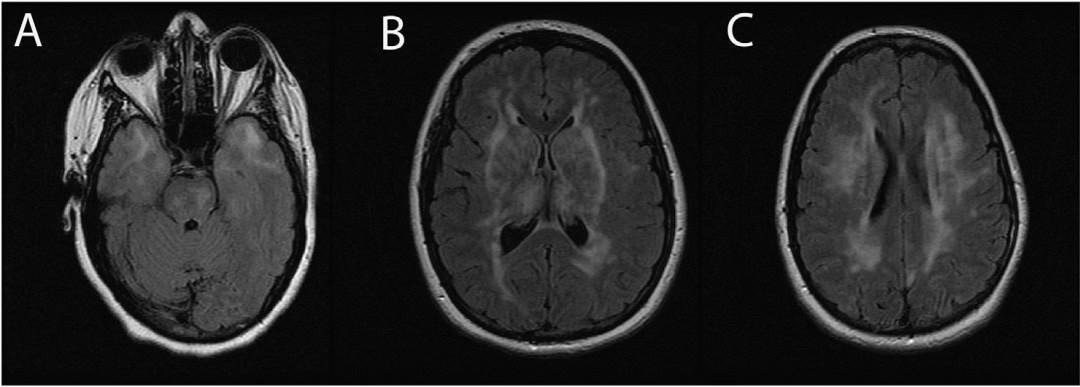
圖7 一例CADASIL患者的資料
A-C:頭顱MRI FLAIR序列顯示前顳葉(A)、外囊(B)和腦室周圍白質(C)T2高信號改變。
圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569.
對於臨床和MRI高度懷疑CADASIL的患者,不管有無典型家族史,最初的確認試驗通常是基因篩查,或者皮膚活檢進行NOTCH3突變免疫組織化學染色;通常不需要也不推薦做腦活檢(圖8)。
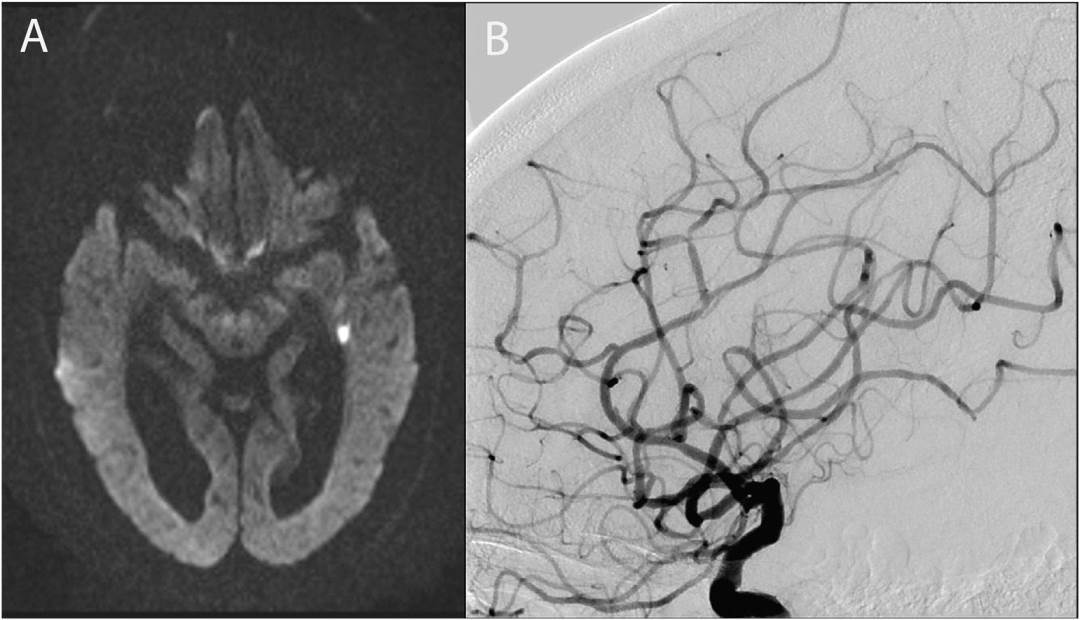
圖8 一例47歲CADASIL患者的資料
A:頭顱MRI顯示雙側有多處慢性皮質下病變,右側內囊有一處急性缺血性病變。B:DSA顯示雙側大腦前動脈(ACA)、大腦中動脈(MCA)和大腦後動脈區域內的多個外周動脈分支節段性狹窄。
皮膚活檢和基因檢測證實為CADASIL。圖片來源Arch Neurol. 2002 Sep;59(9):1480-3.
CADASIL沒有特異性治療,除了典型的卒中二級預防外,沒有特殊的治療方法,主要是抗血小板治療和降低心血管危險因素,如高血壓、膽固醇、吸煙和糖尿病。
07
神經結節病
結節病是一種全身炎症性非肉芽腫性疾病,通常影響淋巴系統和肺部,見於30-50歲人群,女性比例稍高。結節病的病理生理學和病因學尚不清楚,但至少部分是自身免疫性疾病,也與遺傳傾向和某些環境暴露(包括傳染性和毒性)密切相關。當結節病累及神經系統時稱為神經結節病。
神經結節病引起中樞和外周神經病變,包括顱神經麻痹、血管病變、頭痛、神經內分泌功能障礙、腦積水、神經精神症狀、癲癇、脊髓病、神經病變或肌病。以缺血性或出血性疾病或腦靜脈血栓形成為表現形式的卒中相對少見。但在已知結節病的患者或很少或沒有血管危險因素的年輕患者中,神經結節病應該被認為是卒中的一個因素。絕大多數累及腦血管的結節病患者都有活動性神經結節病的其他症狀,特別是腦膜病變。雖然臨床卒中是神經結節病的一種罕見表現,但在屍檢研究中,大多數已知神經結節病患者的中樞神經系統微血管受累,相關的炎症過程可以滲透到內皮細胞壁。
最常見的是,外膜肉芽腫性炎症導致管腔受壓,導致動脈閉塞並導致梗死(圖9A)。頭顱MRI是神經結節病最敏感的檢查方法,可顯示神經結節病的多種表現,包括軟腦膜強化、硬腦膜強化、腫瘤樣病變、累及顱神經的炎症改變、非特異性腦室周圍白質改變或缺血性卒中。由於神經結節病傾向於影響微血管,血管造影檢查通常正常,但有時可能顯示管腔不規則(圖9B)。

圖9 一例神經結節病患者的資料
A:DWI軸位元影像顯示左顳部急性梗死;B:DSA顯示多灶性動脈狹窄。
圖片來源Best Pract Res Clin Rheumatol. 2020 Aug;34(4):101569.
最近研究表明,血管周圍強化和磁敏感偽影(累及腦室周圍靜脈結構,但深部核團不受累)是神經結節病的特徵(圖10)。
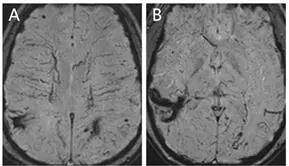
圖10 一例14歲男性神經結節病患者的資料
A和B:SWI 序列顯示皮層下外周多發散在磁敏感偽影,而深部灰質核團不受累。
圖片來源Clin Radiol 2018;73(10):907.e15e23.
LP常常為非特異性炎症表現,包括蛋白升高、細胞增多、寡克隆帶、低血糖和IgG指數升高。與PACNS相比,神經結節病患者的腦脊液更容易出現明顯的細胞增多和低血糖。血管緊張素轉換酶(ACE)敏感性和特異性較低,對診斷價值不大。神經結節病的診斷主要基於活檢病理結果。但由於PACNS和神經結節病都與肉芽腫性炎症有關,因此應努力尋找神經系統外的結節病證據,有助於兩者的鑒別。
神經結節病的治療主要是專家意見,一般初始治療為皮質類固醇。最近有研究報導了英夫利昔單抗用於難治性或嚴重的神經結節病。
08
小結
PACNS是一種威脅生命的疾病,需要迅速識別和治療。由於缺乏敏感和特異性的生物標誌物,明確診斷仍具挑戰。瞭解上述PACNS的mimickers有助於臨床上對PACNS進行診斷。



















